《神经病理学报》:迄今同类最大规模研究发现能逆转APOE4毒性的罕见基因变异!阿尔茨海默病的治疗有望诞生新靶点
来源:代丝雨 2024-05-06 14:08
研究者对筛选出的保护性基因进行基因本体论分析,发现有关细胞外基质(ECM)的各种生物过程富集,例如细胞粘附、整合素结合、ECM结构成分等。
近期,哥伦比亚大学科学团队对四十余万人遗传数据进行了分析,找到了针对APOE ε4的保护突变。研究发现,纤连蛋白1(FN1)的rs140926439变异具有显著AD保护作用(OR 0.29),研究者认为FN1可能是APOE ε4参与AD病理的重要下游机制。
这也是迄今为止规模最大的对AD相关APOE ε4/4携带者的遗传分析。论文发表在《神经病理学报上》。

论文题图
APOE ε4的AD风险根据人种有所不同,在白人、非西班牙裔人群中较非裔美国人、西班牙裔美国人更为突出。
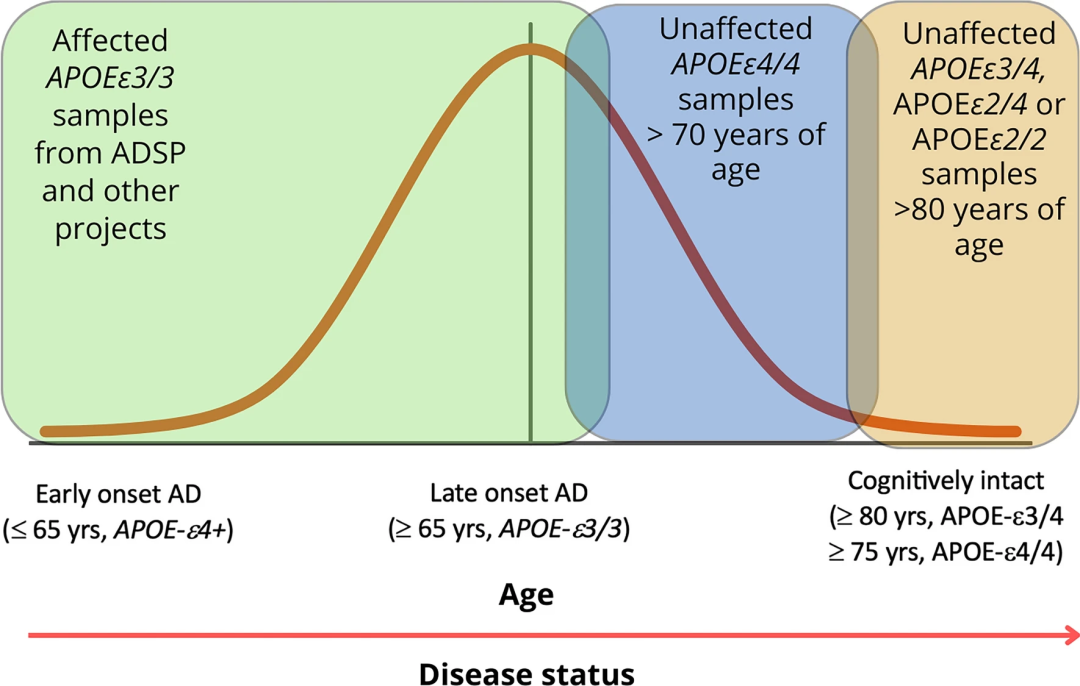
研究者首先分析了来自700个受AD影响的、非西班牙裔白人和加勒比西班牙裔家庭的3578名个体的全基因组分析(GWAS)数据,筛选认知健康的70岁以上APOE ε4纯合子携带者和80岁以上APOE ε4杂合子携带者中存在,而在非携带者中不存在的罕见编码变异(MAF<1%)。
在476个基因中,研究者找到了510个变异,其中尤其值得关注的就是FN1的rs116558455和 rs140926439变体,MAF分别为1.85%和3.33%。
在西班牙裔中,所有携带APOE ε4的AD患者均不携带rs116558455;在非西班牙裔白人中,纯合APOE ε4 AD患者均不携带rs140926439,杂合子患者中仅1%携带。
研究者对筛选出的保护性基因进行基因本体论分析,发现有关细胞外基质(ECM)的各种生物过程富集,例如细胞粘附、整合素结合、ECM结构成分等。研究者猜想,保护机制与ECM有关。
研究者从ECM相关变异中选择了FN1和VI型胶原蛋白α2链(COL6A2),它们是常见的ECM成分。COL6A2 rs777822883和FN1 rs140926439两个变异都涉及带电残基的变化,研究者利用AlphaFold分析蛋白结构,认为二者均会影响蛋白结构稳定性,可以认为它们是功能丧失突变。
为了验证FN1变体的保护作用,研究者调取了多个AD相关的遗传队列,最终纳入了465669名60岁以上非西班牙裔白人病例对照个体。不过在最终分析中,由于数据源中rs116558455非常罕见,仅对rs140926439进行了分析。
这是迄今为止对AD相关APOE ε4/4携带者规模最大的遗传分析。
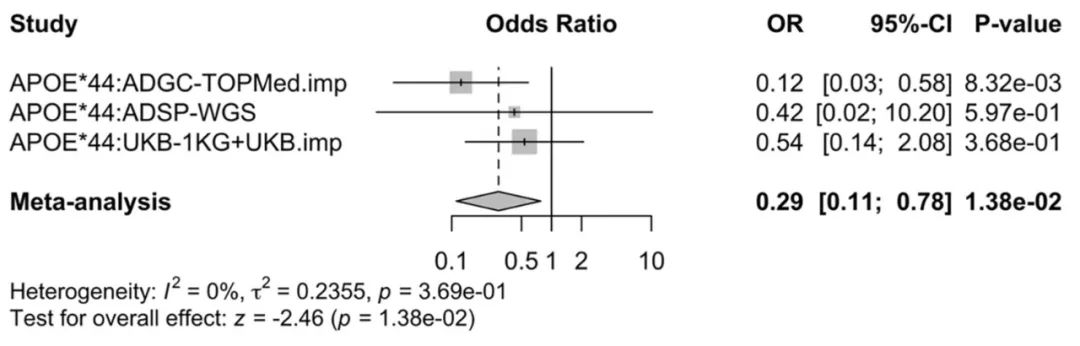
分析结果显示,rs140926439与APOE ε4/4携带者AD风险显著降低有关(OR 0.29),分析发病年龄可发现,单个次要等位基因拷贝可将APOE ε4/4携带者发病延迟3.4年。
FN1主要表达于血脑屏障(BBB)基底膜,研究者认为APOE ε4可能与其沉积水平有关。27名已知APOE基因型的AD患者脑样本分析显示,在APOE ε4/4和APOE ε3/4中,FN1水平显著增加,增幅分别为26.6%和8.1%。
而在患有痴呆和认知正常的APOE ε4/4携带者中,FN1沉积水平也是显著不同的,APOE ε4/4 AD患者FN1沉积和反应性胶质增生水平更高。
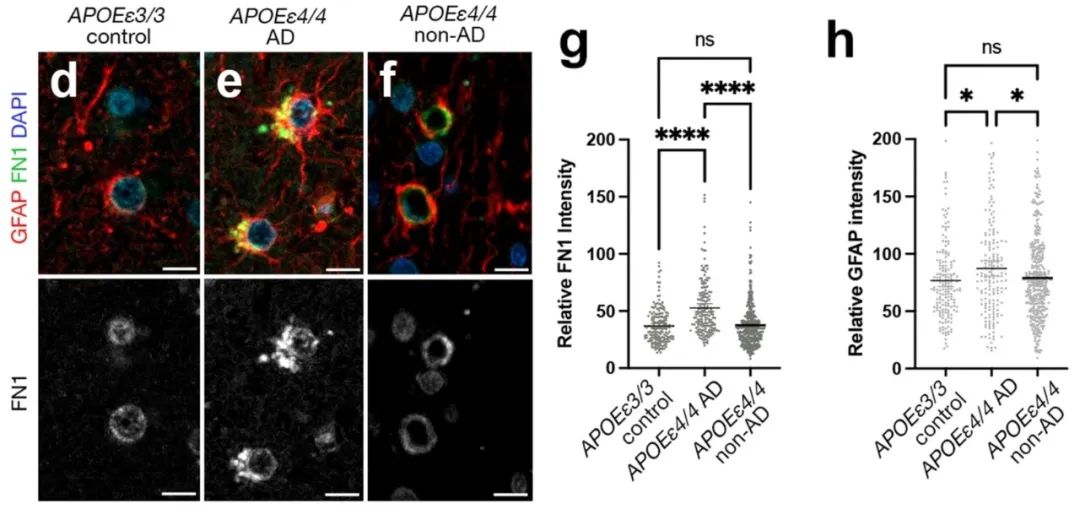
APOE ε4/4 AD患者FN1沉积和反应性胶质增生水平更高
研究者在斑马鱼中测试了FN1的具体功能。敲除斑马鱼fn1b基因后,用Aβ42处理后可见,纤连蛋白功能丧失减少了胶质-血管相互作用,这在其他研究中已被证实是一种针对淀粉样蛋白毒性的保护机制,可以增强对有毒蛋白聚集体的清除和免疫活性。
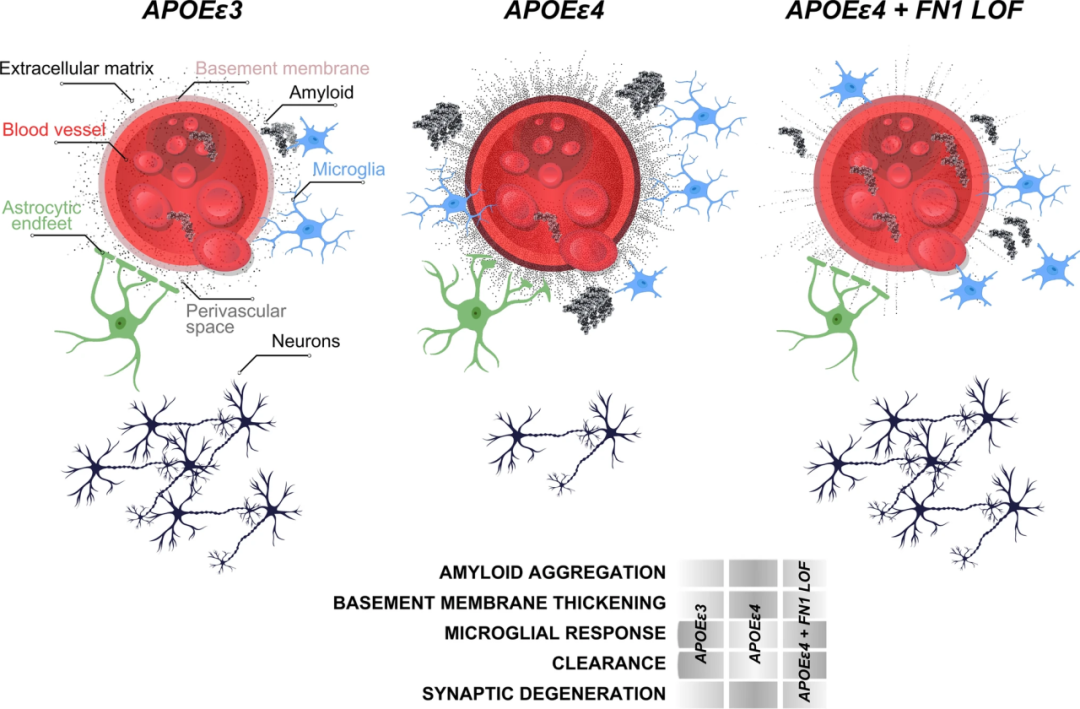
由此可见,纤连蛋白实际上是对β淀粉样蛋白清除的负向调节机制。纤连蛋白为免疫细胞提供了附着点,在病理条件下会损害血管功能、导致血脑屏障分解和突触完整性丧失。
遗憾的是,由于FN1变体在人类患者中相对还是罕见的,研究未能对相应个体进行神经病理学评估,或许更大规模的研究能够提供这个机会。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


